百奥泰:财通证券-百奥泰-688177-公司近况跟踪(二)-250814
-
股票名称百奥泰
-
股票代码688177
-
研报类型(PDF)
-
发布者酷*****
-
研报出处财通证券
-
研报页数3 页
-
推荐评级增持
-
研报大小428 KB
投资标的:百奥泰(688177) 推荐理由:公司在研药品BAT4406F获得微小病变肾病适应症的临床试验批准,且在视神经脊髓炎谱系疾病的临床试验中表现出良好效果,建议提前结束试验。
BAT2506注射液也获得FDA受理,未来收入增长可期,维持“增持”评级。
核心观点1- 百奥泰的BAT4406F注射液获得了针对微小病变肾病/局灶节段性肾小球硬化的临床试验批准,并在视神经脊髓炎谱系疾病的关键临床研究中取得了积极进展。
- BAT2506(戈利木单抗)注射液的上市许可申请已获得美国FDA受理,标志着公司在生物类似药领域的进一步发展。
- 投资建议维持“增持”评级,预计公司未来三年营业收入将稳步增长,但面临研发和商业化的不确定性风险。
核心观点2百奥泰(688177)近期获得药物临床试验批准通知书,针对在研药品BAT4406F注射液新增微小病变肾病/局灶节段性肾小球硬化适应症。
BAT4406F是一种新一代糖基优化的全人源抗CD20抗体,能够通过结合B细胞及前体细胞表面的CD20分子,诱发ADCC和CDC等生物学效应以清除B细胞。
目前BAT4406F已获批的临床试验适应症包括视神经脊髓炎谱系疾病和微小病变肾病/局灶节段性肾小球硬化。
近期在视神经脊髓炎谱系疾病的关键注册II/III期临床研究中,BAT4406F的有效性达到了预设的统计准则,独立数据监查委员会建议提前结束试验,公司决定结束该研究的受试者招募并推进后续工作。
此外,BAT2506(戈利木单抗)注射液的上市许可申请已获得美国FDA受理。
BAT2506是百奥泰开发的戈利木单抗生物类似药,靶向TNF-α,能够阻断TNF-α与其受体的结合,从而抑制其活性。
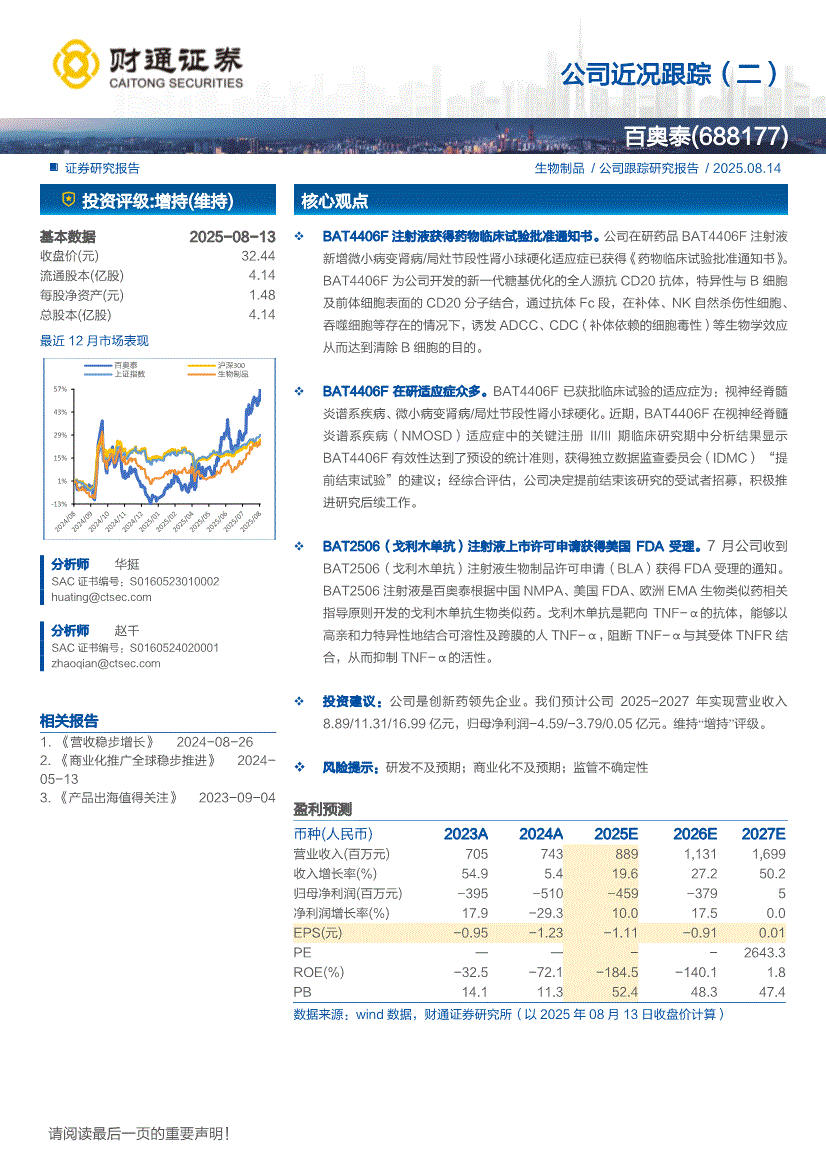
投资建议方面,公司被视为创新药领先企业,预计2025-2027年实现营业收入分别为8.89亿元、11.31亿元和16.99亿元,归母净利润为-4.59亿元、-3.79亿元和0.05亿元,维持“增持”评级。
风险提示包括研发和商业化进展不及预期以及监管不确定性。
- 大家关注
- 1、 东吴证券-周观:从股债性价比角度看债市点位(2025年第35期)-250907
- 2、 罗克韦尔-“气候灯塔”新篇章:气候变化前沿科技最新洞见-240430
- 3、 国联民生证券-伟星股份-002003-2024年度业绩快报点评:业绩成长优异,全球化战略可期-250227
- 4、 东吴证券-耐世特-1316.HK-线控转向/后轮转向重大突破,24H2业绩符合预期-250401
- 5、 中原证券-市场分析:医药电池行业领涨,A股小幅整理-240904
- 6、 克而瑞研究中心-中国房地产行业研报:交付与服务深度融合交付力从“交付产品”向“交付生活”升维-250331
- 7、 开源证券-氟化工行业周报:R32、R22内贸市场货源偏紧,关注制冷剂旺季行情-240519
- 8、 长城证券-远兴能源-000683-阿拉善项目二期启动建设,公司纯碱产能稳步爬坡-240425
- 9、 财通证券-中信博-688408-跟踪支架龙头企业,深耕新兴市场迎放量-240912
- 10、 长城证券-潮宏基-002345-25H1业绩增长亮眼,期间费用率下降带动净利率提升-250905
- 11、 五矿期货-镍周报:矿端消息扰动市场,镍价弱势下跌-250531
- 12、 瑞达期货-甲醇市场周报-250530
- 13、 中泰期货-沪铜周度报告:宏微观预期降温,铜价高位震荡-250324
- 14、 万联证券-晨会-250314
- 15、 天风证券-基础化工行业研究周报:3月份化学原料和化学制品制造业增加值同比增长8.8%,三氯乙烯、三氯蔗糖上涨-250421
- 16、 华金证券-赛分科技-688758-新股覆盖研究-241222
- 17、 山西证券-新能源动力系统行业固态电池深度报告:聚焦性能和成本,固态电池产业化提速-241022
- 18、 国金证券-恒林股份-603661-利润短期承压,期待后续高质量发展-250426
- 19、 中原证券-华工科技-000988-公司点评报告:净利润快速增长,海外业务拓展顺利-250717
- 20、 国投证券-有色金属行业周报:博弈关税政策金属价格震荡,国内关注节后需求兑现情况-250128
- 21、 瑞达期货-焦煤市场周报:宏观扰动远月涨停,盘面宽幅震荡运行-250905
- 22、 天风证券-百济神州-688235-2024Q2公司业绩表现超预期,实现非GAAP经营利润盈利-240815
- 23、 东方证券-社会服务行业周报:服务类消费继续领跑实物商品,入境游热度攀升-240722
- 24、 光大证券-新兴铸管-000778-2023年年报业绩点评:业绩追随行业有所下滑,期间费用率下降显著-240414
- 25、 西南证券-鼎捷数智-300378-大陆收入提速,AI商业化持续领先-241104
- 26、 华安证券-联影医疗-688271-国产医疗影像设备先驱,创新引领志在全球发展-240918
- 27、 西南证券-伊力特-600197-疆外自营提能蓄力,关注改革落地成效-250428
- 28、 东方证券-机械设备行业机器人产业跟踪:宇树科技开启上市辅导,国内人形机器人加速落地预期有望加强-250720
- 29、 华西证券-名创优品-9896.HK-兴趣消费引领者,全球扩张正当时-240930
- 30、 民生证券-孩子王-301078-2024年半年报点评:Q2扣非利润稳健增长,开拓主品牌加盟业态进一步打开增量空间-240816







